6月10日傍晚5點,高端疫苗二期臨床試驗結果解盲。整場記者會中,「中和抗體效價」「免疫橋接」等專有名詞,一般人很難聽懂。總體而言,這款疫苗的安全性與耐受性良好,抗體濃度也有一定數值。下一步,就看疫苗審查委員給不給過,而委員們看的卻是AZ這一關?
戰勝這場不知何時結束的新冠疫情,國產疫苗是否能為台灣抗疫工作增加一些「籌碼」?也使得高端疫苗二期臨床主試驗的期間分析解盲結果,成為重要的依據。
高端疫苗發言人、執行副總李思賢表示,根據解盲結果的數據顯示,該新冠疫苗的安全性與耐受性良好,所有受試者未出現疫苗相關嚴重不良反應。
其次,在免疫生成性部分,不區分年齡組情況下,疫苗組在施打第二劑後28天的血清陽轉率(seroconversion rate)達99.8%,而20~64歲的疫苗組,血清陽轉率則為99.9%,顯示兩組受試者在接受兩針疫苗施打後,幾乎全數成功誘發免疫反應。
再來觀察的指標是「中和抗體的幾何平均效價」,英文稱之為GMT titer,用一般人聽得懂的白話文翻譯,其實就是體內抗體的濃度。在不區分年齡組,其數值為662,GMT倍率比值為163倍增加。而20~64歲的疫苗組,中和抗體效價則為733,GMT倍率比值為180倍增加。
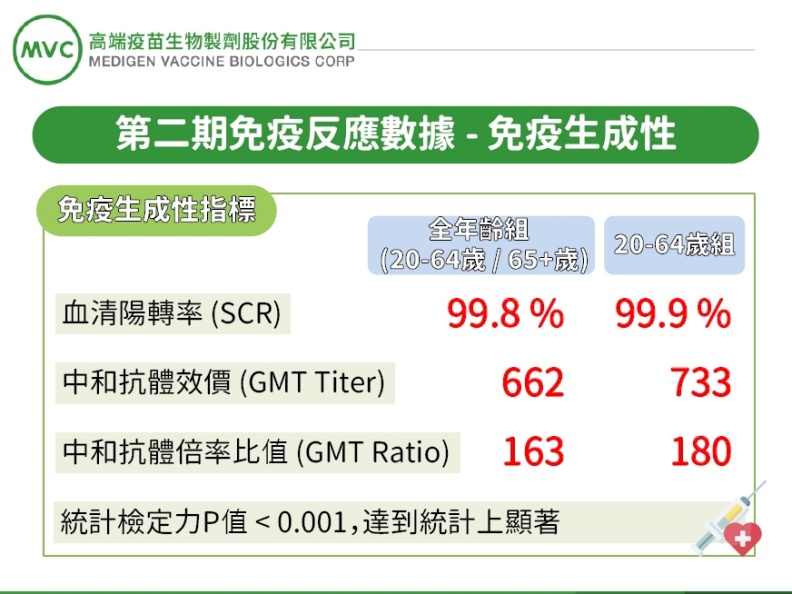
另外在次要評估指標中的批次一致性研究中,數據也顯示本次臨床試驗的疫苗,生產時的製程穩定。
是否覺得以上描述,說的不是人話?簡單歸納就是,高端宣稱,該疫苗接種後顯現了良好的安全性,接種疫苗組受試者均產生了一定濃度的中和抗體,而且每一支疫苗的品質都一樣。
從以上數據,高端判定這次的二期臨床實驗算是成功。
以「免疫橋接」取代傳統三期試驗
不過,疫苗研發之路尚未結束。相關數據還得送交主管機關申報,由食藥署邀請國內臨床、統計、藥毒理、製造研發及公衛等相關專業領域的專家學者,召開「疫苗審查委員會」進行審查。
眾多指標中,最受關切的便是中和抗體效價的數據,因為它會被特地挑出來,作為食藥署是否核准「緊急使用授權」(EUA)的評判依據。
不尋常的是,就在高端解盲當天的前幾個小時,食藥署才突然公告了國產COVID-19疫苗EUA的審查標準。
食藥署在新聞稿中表示,從年初即開始思考如何支持國產疫苗療效,為此,食藥署於第一批AZ疫苗在三月於國內開始接種時,便委託部立醫院執行研究計畫,蒐集200位國人接種AZ疫苗的中和抗體效價作為外部對照組。
同步,食藥署並於5月初起陸續召開專家會議討論,研商以免疫橋接(immuno-bridging)的方式,採用中和抗體作為替代療效指標,衡量國產疫苗誘發產生的免疫原性結果、是否與國人接種國外已核准EUA的疫苗相當,作為支持國產疫苗療效的佐證。
食藥署還指出,國產疫苗第二期臨床試驗所得中和抗體效價,必須證明不劣於AZ疫苗。
但在新聞稿的附件中,卻特別標示了一條但書:「若申請EUA前WHO釋出中和抗體之保護力相關指標的閾值數據,則參考WHO標準設定血清反應率的比較條件。」

能否取代三期?國產疫苗要先與AZ疫苗PK!
事實上,世界衛生組織(WHO)已於5月26日開過專家會議,提出以免疫橋接研究取代傳統三期臨床試驗的討論,但至今沒有定論,也尚未公佈中和抗體濃度絕對數值的標準為何。
高端疫苗生物製劑廠廠長連偉成,同時也有醫師身份,則在記者會中表示,以免疫橋接替代三期臨床的作法在國際上也有先例,比如Novavax在英國的一次嘗試。
最後如果證明中和抗體的濃度果然夠濃,就代表這款疫苗對人體具備抗擊COVID-19病毒的保護力?接著真的能施打在國人身上了嗎?許多專業醫師及科學家不認為如此。
一位不具名的免疫學專家就指出,AZ是腺病毒載體疫苗,高端疫苗是次單位疫苗,兩者的技術方法不同,「請問可以就這樣比較兩者的免疫原性嗎?」這樣的論述,與辭去疫苗審查委員一職的中研院院士陳培哲看法類似。
前台大感染科醫師「林氏壁」也在看完解盲記者會後對《遠見》表示:「高端測出這個中和抗體的效價,不要和Novavax 那幾千的效價比較啦!實驗室不同,方法不同,無法直接比較喔。」
高端愈解愈茫?就讓專家來吧!
但也有另一派意見認為:「讓科學回歸科學。」
陽明交大公衛所兼任教授、首任疾管局局長、前健保局總經理張鴻仁表示,到底現在國產疫苗的兩家公司高端疫苗、聯亞生技,所執行的擴大型二期臨床,免疫橋接符合不符合國際規範?「讓專家去判斷。」
張鴻仁所謂的專家,是疫苗審查委員會的成員。據他對審查體系的了解,這群審查專家是國內的領先專家,擁有一定的學術地位,以他知曉的內情,常有新藥公司、生技公司批評食藥署邀請的專家:「只聽過審查太嚴格,很少聽說抱怨太鬆的。」
「重點是,他們也從來不聽食藥署長的,更不必講是食藥署的長官,我們的專家都很可愛,政治力的因素不可能影響這些審核的專家,大家可以拭目以待,」張鴻仁說。